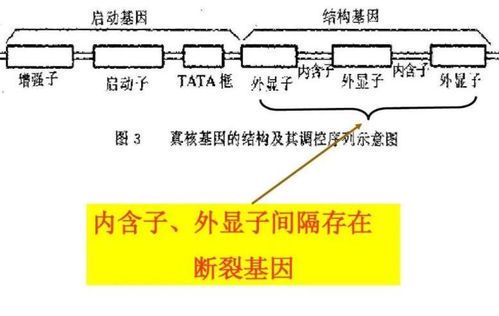
在分子生物学领域,断裂基因(split gene)是指编码区被非编码序列隔断的基因结构。这种特殊排列方式于1977年由Sharp和Roberts团队首次在腺病毒中发现,彻底改变了人们对基因连续性的传统认知。断裂基因的发现为真核生物基因表达调控研究开辟了新方向。
典型断裂基因由外显子(exon)和内含子(intron)交替组成。外显子作为最终保留在成熟mRNA中的编码序列,平均长度约150bp;而内含子作为转录时被剪除的非编码序列,长度差异可达数十倍。人类基因组中约94%的基因属于断裂基因,其中平均每个基因包含8.8个内含子,最著名的案例是长达240万个碱基的肌营养不良蛋白基因(DMD)。
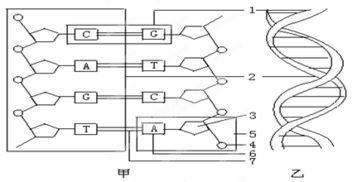
从结构特征来看,断裂基因在DNA序列上存在明显的剪接信号。内含子5'端通常以GU开始(供体位点),3'端以AG结束(受体位点),分支点序列则位于内含子内部。这些保守序列与剪接体复合物共同构成精确的剪接机制,确保外显子的正确拼接。值得注意的是,约1%的断裂基因存在选择性剪接现象,使得单个基因可产生多种蛋白质变体。
进化生物学研究表明,断裂基因可能源于早期基因重组事件。内含子的存在既增加了遗传变异的可能性,也为外显子洗牌(exon shuffling)提供了物质基础。比较基因组学数据显示,低等真核生物如酵母的断裂基因数量显著少于高等生物,暗示基因断裂化可能与生物复杂性进化相关。
当前对断裂基因的研究已延伸至医学应用领域。约15%的人类遗传病与剪接异常相关,如β-地中海贫血就常由剪接位点突变引起。新一代基因治疗技术如CRISPR-Cas9,正尝试通过精准修饰断裂基因结构来治疗相关疾病。未来随着三维基因组学的发展,对断裂基因空间构象与功能关系的理解将更加深入。